Im folgenden werden die wichtigsten chemische Grundlagen erläutert, die für die Schule und das Studium wichtig sind. Dabei handelt es sich um Redoxreaktionen, Säure-Base-Reaktionen und die Phasentrennung.
Redoxreaktionen
1) Wie erkenne ich eine Redoxreaktion?
An einer Änderung der Oxidationszahl! Das bedeutet, dass bei dieser Reaktion Elektronen übertragen werden. Insbesondere Metalle haben eine große Bandbreite: Fe/Fe2+/Fe3+ Cu/Cu+/Cu2+ Mn/Mn2+/Mn4+/Mn7+
Aber auch die Nichtmetalle (C,N,P,S) haben viele unterschiedliche Verbindungen, was in der Natur sehr bedeuted ist. Änderung des Stickstoffs (N) : N2/NH3 oder NH4+/NO2–/NO3– (Stickstoffkreislauf)
2) Aufstellen der Teilgleichungen
Es muss immer Ladungsneutralität herrschen: die Gesamtladung (Addition aller Teilladungen) ist 0
Reduktion: Verkleinerung der Oxidationszahl 0,5 O2 + 2 e- > O2-
Oxidation: Erhöhung der Oxidationszahl Fe > Fe3+ + 3 e-
3) Aufstellen der Gesamtreaktion
Die Anzahl der übertragenen Elektronen in Reduktion und Oxidation müssen gleich sein (Gleichgewicht). Deshalb werden die Teilreaktionen nach dem kleinsten gemeinsamen Vielfachen ausgeglichen!
Reduktion: 2e- x 3 = 6 e- Oxidation: 3e- x 2 = 6 e-
Alle Elemente der Teilgleichung werden nun mit dem kleinsten gemeinsamen Vielfachen multipliziert.
1,5 O2 + 6 e- + 2 Fe > 3 O2- + 2 Fe3+ + 6 e-
Die Elektronen sind vor und nach der Reaktion gleich und werden gekürzt. Eine stabile Verbindung des Eisenoxids ist entstanden.
1,5 O2 + 2 Fe > Fe2O3
Säure-Base Reaktionen
Zu den chemischen Grundlagen gehören Säure-Base Reaktionen, wo die Autoprotolyse des Wassers entscheidend ist. Die Dissoziation in Protonen H+ (Hydroniumionen ist präziser) und zeigt die saure Eigenschaft des Wassers (Protonendonator). Wiederum sind die entstandenen Hydroxidionen OH– in der Lage, Protonen an sich zu binden (Protonenakzeptor).
H2O > H+ + OH–
Bei einem neutralen pH Wert von 7 liegen die Protonen und Hydroxidionen in gleicher Konzentration vor (Gleichgewicht). Durch verschieden starke Säuren (pKS) oder Basen (pKB) kann dieses Gleichgewicht verschoben werden.
Grundlagen der Phasentrennung
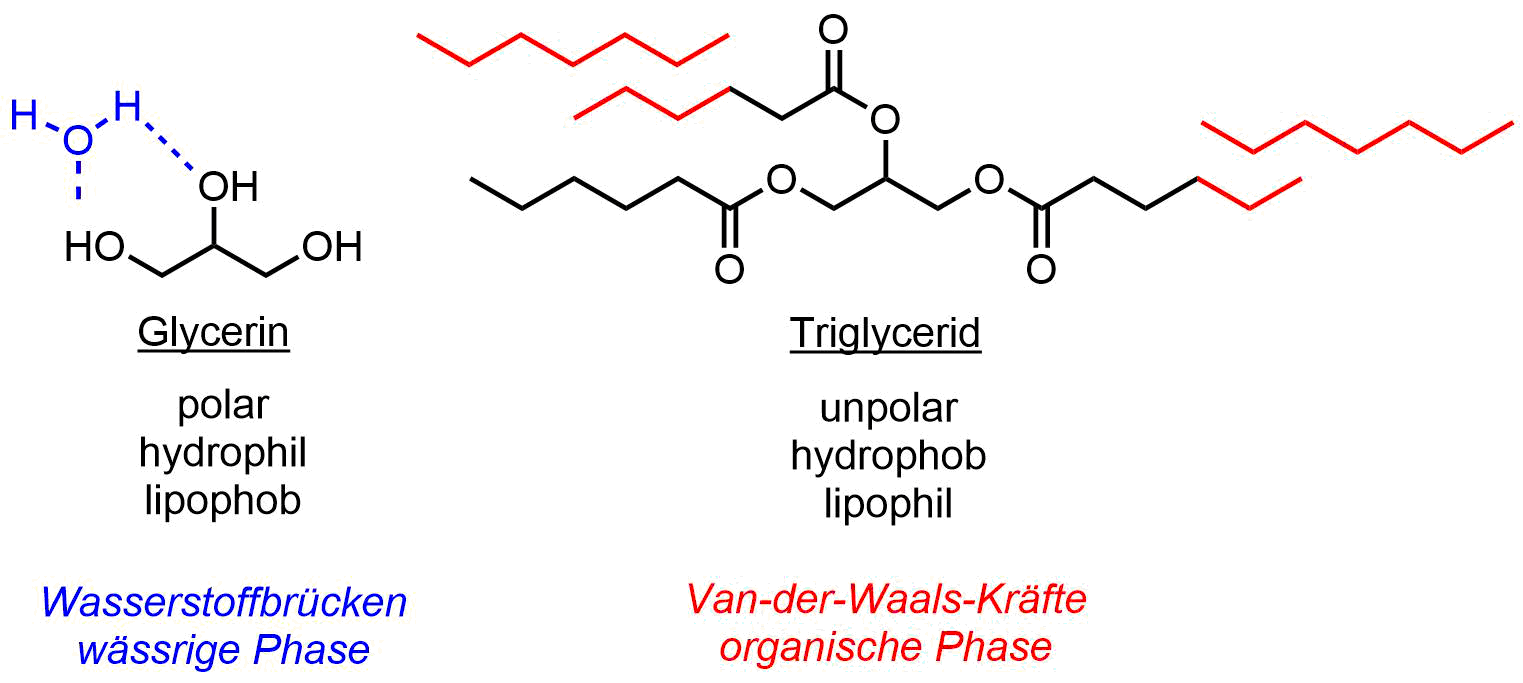
Die Fettaugen auf einer Suppe oder der Ölfilm auf einem Gewässern sind Beispiele für dieses Phänomen. Hauptverantwortlich dafür sind die attraktiven Wechselwirkungen ähnlicher Moleküle zueinander. Das sind zum einen polare Verbindungen, die Wasserstoffbrücken aufbauen in einer wässrigen Phase. Zum anderen sind es Van-der-Waals-Kräfte von unpolaren Molekülen in der organischen Phase. Die repulsiven Wechselwirkungen der beiden Phasen führen dann zur Phasentrennung. Das Phänomen kann am Beispiel des polaren Glycerins und unpolaren Triglycerid verdeutlicht werden. Je länger die unpolare Kette des Triglycerids wird desto mehr steigen die Van-der-Waals Kräfte und damit steigen die abstoßenden Kräfte zur wässrigen Phase, was zur Phasentrennung führen kann.
Quellen
[1] www.leifichemie.de/redoxreaktionen-und-elektrochemie/redoxreaktionen-als-elektronenuebertragungen
